Hoy en día no existen tratamientos específicos para el MCA, aun así, los últimos avances de la terapia génica en algunas enfermedades de la retina (amaurosis congénita de Leber y coroideremia) lo convierten en una enfermedad que podría beneficiarse de ella.
La terapia génica consiste en una inyección en la retina en la cual, empleando como vector un virus incapaz de reproducirse (y por lo tanto de provocar efectos dañinos), se introduce un gen específico en las células del enfermo. El virus inyectado en la retina infecta los conos en los que introduce la secuencia génica correcta, que es la misma que se encuentra en un individuo sano. Esta secuencia no substituye la mutación del gen en el núcleo de los conos del enfermo, sino que introduce la proteína omitida dentro del segmento externo de los conos y corrige de esta forma el defecto.
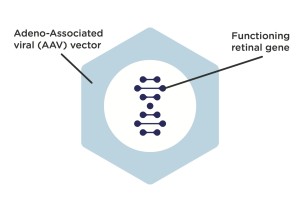
Paso 1: los científicos modifican un virus adenoasociado (AAV) – un virus común del que no se sabe cause ninguna enfermedad en humanos – eliminando lo que hay en el interior del virus y sustituyéndolo por una copia funcional de un gen de L-opsina o M-opsina.
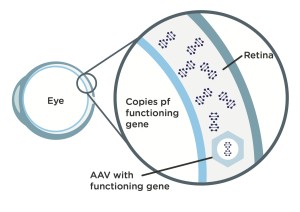
Paso 2: cuando los médicos inyectan por vía intravítrea el vector modificado (AAV) en el ojo de un paciente, éste viaja hasta las células de los conos de la retina del paciente. Una vez dentro de los conos, el vector transmite la copia funcional del gen de la L-opsina o de la M-opsina que necesita el paciente con MCA y que estaba alojada en el vector AAV.
La corrección efectuada con la terapia génica no se «transmite» a los hijos y nietos. Por este motivo, las personas que han heredado la enfermedad deben volver a seguir el tratamiento.
En el caso de la amaurosis congénita de Leber y de la coroideremia, tras estudios en laboratorio y pruebas de eficacia en modelos animales, se han activado ensayos clínicos en los que se han tratado con éxito muchos enfermos de diferentes países.
En lo que respecta al MCA, los investigadores han creado un modelo animal en el que realizaron pruebas de terapia génica.
Para saber más sobre la terapia génica y los virus adenoasociados, consulte la siguiente página web.
Un modelo animal para el MCA
La BCM Families Foundation ha creado un nuevo modelo animal, el ratón BCM C198R. Esta línea de ratones se creó con tecnología CRISPR, que se utilizó para replicar con precisión la mutación puntual de cisteína-203 a arginina (C203R) que se encuentra en los genes de opsina del cono LWS/MWS humanos. La diferencia en la numeración de 198 frente a 203 refleja la diferente longitud de las proteínas humanas y de ratón. Esta mutación por sustitución de aminoácidos es responsable del Monocromatismo de Conos Azules en aproximadamente la mitad de las personas que padecen la enfermedad en todo el mundo.La línea de ratones BCM C198R es el primer modelo animal disponible para estudiar los mecanismos patogénicos específicos asociados con el Monocromatismo de Conos Azules y probar posibles enfoques terapéuticos.A partir de septiembrede 2018, los ratones C198R están disponibles en el Laboratorio Jackson (número de pieza 031385). Encuentre más información sobre el mouse BCMFF-C198R aquí BCMFF-C198R o solicite más información por correo electrónico a: info@BCMFamilies.org.
A continuación se muestran algunos artículos de investigación sobre terapia génica en un modelo animal con MCA:
Deng WT, Li J, Zhu P, Freedman B, Smith W C, Baehr W, Hauswirth W W. ‘Rescue of M-cone Function in Aged Opn1mw−/− Mice, a Model for Late-Stage Blue Cone Monochromacy’. Investigative Ophthalmology & Visual Science August (2019) Vol.60, 3644-3651. PMID: 31469404.
Deng WT, Li J, Zhu P, Chiodo V A, Smith W C, Freedman B, Baehr W, Pang J, Hauswirth W W. ‘Human L- and M-opsins restore M-cone function in a mouse model for human blue cone monochromacy’. Molecular Vision (2018) 24, 17-28. PMID: 29386880.
Zhang Y, Deng WT, Du W, Zhu P, Li J, Xu F, Sun J, Gerstner C D, Baehr W, Boye Sanford L, Zhao C, Hauswirth W W, Pang J. ‘Gene-based Therapy in a Mouse Model of Blue Cone Monochromacy’. Scientific Reports. 2017 7 (6690). PMID: 28751656.
Xie B, Nakanishi S, Guo Q, Xia F, Yan G, An J, Li L, Serikawa T, Kuramoto T, Zhang Z. ‘A novel middle-wavelength opsin (M-opsin) null-mutation in the retinal cone dysfunction rat’. Exp. Eye Res. (2010) 91 (1):26-33. PMID: 20371244.
Zhang Z, Pang J, Xia F, Guo Q, Li L, An J, Zhang L, Hauswirth W W, Yang S, Li Z. ‘AAV-mediated Gene Therapy Restores Cone Function In A Rat With An M-cone Opsin Deficiency. A Model For Blue Cone Monochromacy’. ARVO Annual Meeting Abstract 2011.
A continuación enumeramos algunos artículos relacionados con un resultado de la terapia génica en el daltonismo en primates:
Mancuso K, Hauswirth W W, Li Q, Connor T B, Kuchenbecker J A, Mauck M C, Neitz J, Neitz M, ‘Gene therapy for red-green colour blindness in adult primates’. Nature (2009);461:784-787. PMID: 19759534.
Mancuso K, Mauck M C, Kuchenbecker J A, Neitz M, and Neitz J. ‘A Multi-Stage Color Model Revisited: Implications for a Gene Therapy Cure for Red-Green Colorblindness’. (2010) R.E. Anderson et al. (eds.), Retinal Degenerative Diseases, Advances in Experimental Medicine and Biology 664. PMID: 20238067.